Pathologie - Toxicologie
-
Toxicocinétique - Métabolisme [12-15]
L’acétate d'éthyle est bien absorbé par inhalation et ingestion, rapidement hydrolysé et excrété dans l’air expiré et l’urine.
Chez l'animal
Absorption
L'acétate d'éthyle, après inhalation, se dépose dans le tractus respiratoire supérieur (10 à 35 % chez le rat, 36 à 72 % chez le hamster). Du fait de sa bonne solubilité dans le plasma, il traverse facilement la barrière alvéolo-capillaire. Son absorption par voie pulmonaire est donc rapide et importante. Une inhibition des carboxylases diminue le dépôt chez les deux espèces [12]. La substance est également bien absorbée par voie digestive et probablement par voie cutanée (taux d'absorption calculé in vitro : 1,14 mg/cm2/h).
Distribution
L'acétate d'éthyle est largement distribué dans l'organisme par la circulation sanguine. Il a été détecté dans le cerveau de rat après inhalation d'une concentration de 5% pendant quinze minutes.
Métabolisme
Les taux sanguins d'acétate d'éthyle diminuent rapidement (20 % en 8 heures) [14].
Il est rapidement hydrolysé, soit spontanément, soit par l'action d'estérases non spécifiques dans la cavité nasale, le plasma et le foie, en éthanol et en acide acétique. Ces deux produits se transforment principalement en acétyl-coenzyme A, qui est normalement oxydé dans le cycle tricarboxylique et accessoirement dégradé par la voie de cétogenèse qui conduit à la formation d'acide acétylacétique, d'acide p-hydroxybutyrique et d'acétone. Le taux d'acétate d'éthyle transformé dans le tractus respiratoire supérieur est plus important chez le hamster (63 - 90 % de la dose déposée) que chez le rat (40 - 65 %) [12]. À concentrations élevées, le taux d'hydrolyse de l'acétate d'éthyle semble dépasser les capacités de l'organisme à oxyder l'éthanol, entraînant l'accumulation de celui-ci dans le système vasculaire [13].
Schéma métabolique
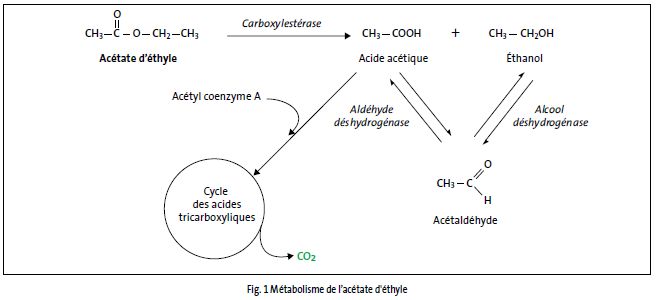
Excrétion
L'élimination de l'acétate d'éthyle est rénale et pulmonaire.
Il est excrété pour une très faible part (< 0,2 %) sous forme inchangée par voie respiratoire avec une demi-vie d'élimination de 9 minutes. Le reste est éliminé sous forme métabolisée dans les urines [14].
Chez l'Homme
Le métabolisme de l'acétate d'éthyle est identique à celui de l'animal. Le taux de rétention pulmonaire est de 50 à 60 % après l'inhalation de concentrations variant de 94 à 137 ppm chez des volontaires. L'exposition se traduit par une augmentation de la concentration de l'ester, d'éthanol et éventuellement d'acétone dans le sang. Des études ont été menées chez des volontaires exposés en chambre d'inhalation à des concentrations comprises entre 217 et 770 ppm, pendant des durées variables de 0,7 à 5 heures. La concentration d'acétate d'éthyle dans l'air alvéolaire pendant et après l'expérimentation est directement proportionnelle à la durée de l'exposition, alors qu'elle n'est pas influencée par le niveau de celle-ci [15]. En raison de la transformation rapide de l'acétate d'éthyle dans l'organisme, la concentration d'éthanol dans l'air alvéolaire augmente fortement durant l'expérimentation et proportionnellement à la concentration de l'exposition. D'autre part, le niveau d'acétone dans l'air alvéolaire n'est pas influencé de façon significative par l'absorption d'acétate d'éthyle. Après arrêt de l'exposition, les concentrations alvéolaires en acétate d'éthyle et en éthanol diminuent rapidement ; la courbe d'élimination pulmonaire n'est en rapport qu'avec les derniers instants de l'exposition et varie d'un individu à l'autre : elle ne représente donc pas une bonne estimation de l'importance d'une longue exposition.
D'autres auteurs ont montré qu'une exposition de 400 ppm (1400 mg/m3) d'acétate d'éthyle engendrait en fin de période de travail une concentration alvéolaire de solvant de 168 mg/m3.
La rétention respiratoire de l'acétate d'éthyle est plus élevée que celle d'autres solvants tels que le toluène, le trichloréthylène, le benzène, l'acétone, l'éthanol et l'hexane; l'élimination pulmonaire est pratiquement négligeable comparée à celle de ces autres solvants [11].
Surveillance Biologique de l'exposition
Les dosages de l'acétate d'éthyle sanguin immédiatement en fin de poste et urinaire en fin de poste et fin de semaine de travail ont été utilisés pour la surveillance biologique de l'exposition, mais il n'existe que peu de données dans la littérature sur la pertinence de ces paramètres.
Il n'existe pas de valeurs guides pour ces indicateurs [14].
-
Mode d'actions
-
Toxicité expérimentale
Toxicité aiguë [1, 2, 5]
L’acétate d'éthyle est faiblement toxique pour l’animal ; il est irritant pour le tractus respiratoire supérieur et les yeux mais n’est pas sensibilisant.
Voie d'administration Espèce CL50 / DL50 Inhalatoire Rat
Souris
14 640 ppm (durée non connue) ;
Exposition de 6 heures : CL0 = 8000 ppm ; CL100 = 16 000 ppm.
44 000 mg/m3 (12 225 ppm) pendant 3 heures
Orale Rat
Souris
Cobaye
Lapin
5620 à 10 200 mg/kg
4100 à 4400 mg/kg
5500 mg/kg
4935 - 7650 mg/kg
Cutanée Lapin > 18 000 mg/kg Tableau I. Toxicité aiguë de l'acétate d'éthyle.
La toxicité aiguë de l'acétate d'éthyle est faible quelle que soit la voie d'exposition.
Chez la souris et le cobaye, exposés par voie orale à forte dose, on observe un effet dépresseur du système nerveux central se traduisant par une somnolence, des troubles moteurs et un coma.
Après exposition par inhalation, l'importance des effets observés et leur évolution sont fonction des concentrations auxquelles les animaux sont exposés :
- l'inhalation de vapeurs saturées est létale au-delà de 15 minutes ;
- à fortes concentrations, à partir de 12 000 ppm pendant 5 heures chez le chat et de 5000 ppm pendant 4 heures chez la souris, l'acétate d'éthyle exerce une toxicité neurologique centrale, marquée par des troubles de coordination, une somnolence, puis un coma. Aux doses les plus élevées, les animaux morts présentent un œdème pulmonaire hémorragique avec hyperhémie du tractus respiratoire. Une anémie et une atteinte hépatique sont également observées chez le chat exposé à 43 000 ppm, pendant 14 à 16 minutes ;
- aux concentrations plus faibles, on observe une irritation des muqueuses. Une irritation oculaire et nasale avec dyspnée apparaît chez la souris après une exposition de 17 heures à une concentration atmosphérique de 2000 ppm ; une atteinte de la cornée est constatée pour des concentrations plus élevées (5000 ppm, pendant 3 à 4 heures et 10 000 ppm, pendant 45 minutes). Chez la souris, au-delà de 2000 ppm, on observe des modifications neuro-comportementales (modification de posture, augmentation des mouvements toniques, retard des réflexes posturaux, réactivité sensori-motrice augmentée), réversibles dès l'arrêt de l'exposition [16].
La toxicité de l'acétate d'éthyle diminue s'il est mélangé à du toluène, et la toxicité du mélange est moindre que celle de chacun des deux composants pris isolément. La DL 50 de l'acétate d'éthyle est diminuée s'il est mélangé à de l'oxyde de propylène, du propylène glycol ou du formol, augmentée s'il est associé à de la morpholine, de l'éthylène glycol ou de l'éthanol.
Irritation - Sensibilisation
L'instillation oculaire de 2 gouttes d'acétate d'éthyle chez le lapin, suivie, 2 minutes plus tard, d'un rinçage à l'eau, entraîne immédiatement une rougeur et un discret œdème conjonctival ainsi qu'une atteinte microscopique de l'épithélium cornéen ; l'évolution spontanée vers la guérison est obtenue en 1 à 2 jours.
L'acétate d'éthyle n'est pas sensibilisant pour le cobaye dans le test de maximisation.
Toxicité subchronique, chronique [1]
Une exposition prolongée à l’acétate d'éthyle induit un effet sédatif transitoire et une baisse de poids corporel et des organes.
L'exposition par inhalation (rat, 350-750-1 500 ppm, 6 h/j, 5 j/sem., pendant 94 jours) engendre aux deux plus fortes concentrations une baisse de la prise de poids et de nourriture et du taux de triglycérides ; aucune modification clinique, spermatique ou ophtalmologique n'est notée. Une diminution de la réponse au stimulus d'alerte est observée pendant l'exposition uniquement ; elle serait la conséquence de l'effet sédatif transitoire de l'acétate d'éthyle. À l'examen microscopique, on observe une dégénérescence de la muqueuse olfactive nasale de minimale à sévère selon la concentration. La NOEL est 350 ppm (1,2 mg/L). À de plus fortes concentrations (rat, 1500 - 3000 - 6000 ppm, 6 h/j, 5 j/sem. pendant 2 semaines), l'animal présente hypoactivité, blépharospasme, perte du réflexe d'alerte, baisse de poids corporel, augmentation de poids des poumons (2 sexes, 6000 ppm) et diminution de poids de la rate (mâles, ≥ 3000 ppm) et des ovaires (femelles, 6000 ppm).
L'exposition répétée de cobayes (2000 ppm, 4 h/j, 6 j/sem.) n'entraîne pas de symptomatologie après 65 expositions. Des expositions par voie orale (rat, gavage, 0 - 300 - 900 - 3600 mg/kg/j pendant 90 jours) provoquent une diminution de prise de nourriture, du poids corporel et du poids des organes chez les mâles ; l'effet n'est pas significatif chez les femelles. La NOEL est de 900 mg/kg/j.
Effets génotoxiques [1]
L’acétate d'éthyle n’est pas mutagène pour les bactéries ; c’est un clastogène douteux in vitro et négatif in vivo dans les conditions des tests pratiqués.
L'acétate d'éthyle n'est pas mutagène dans le test d'Ames sur 6 souches de Salmonella typhimurium, avec ou sans activation métabolique. Il induit des aberrations chromosomiques sur cultures de fibroblastes de hamsters chinois sans activation métabolique (résultats douteux à 24 heures, positifs à 48 heures), mais pas sur cellules ovariennes de hamster chinois avec et sans activateurs métaboliques ; en revanche, chez ces dernières, il augmente le taux des échanges entre chromatides sœurs.
Dans un essai sur une souche de Saccharomyces cerevisiæ, l'acétate d'éthyle s'est révélé inducteur d'aneuploïdie mitotique (malségrégation chromosomique) mais n'a pas entraîné de recombinaison mitotique ou de mutation ponctuelle.
In vivo, le test du micronoyau est négatif chez la souris (100 - 200 - 400 - 800 mg/kg, intrapéritonéal (i.p)) et le hamster (473 mg/kg, i.p ou 2500 mg/kg, gavage).
Effets cancérogènes [1]
L’acétate d’éthyle n’induit pas de développement tumoral dans les conditions des tests pratiqués.
L'administration intrapéritonéale d'acétate d'éthyle chez des souris (74 injections réparties sur 8 semaines, avec une dose totale de 3600 et 18 000 mg/kg) n'entraîne pas d'excès de tumeurs pulmonaires après 24 semaines d'observation.
Des rats, exposés par inhalation (350 - 750 - 1500 ppm, 6 h/j, 5 j/sem, 94 jours), ne présentent pas de lésion macroscopique ou microscopique ; seule une dégénérescence de la muqueuse olfactive nasale a été rapportée.
Effets sur la reproduction [1, 17]
L’exposition à l’acétate d'éthyle modifie le poids des testicules, les effets sur le sperme varient selon les auteurs.
Une exposition par inhalation de rats à une concentration de 17,6 % (2 fois/jour, 4 à 6 minutes pendant 7 jours) entraîne une baisse significative du poids du corps et des testicules. Les auteurs ont également observé au niveau de la prostate une baisse d'activité de la phosphatase acide, ainsi qu'un taux plus bas de testostérone plasmatique, par comparaison aux valeurs du groupe témoin. L'acétate d'éthyle a également entraîné une diminution du taux de spermatozoïdes de l'épididyme. En revanche, l'exposition de rats mâles à 350 - 750 - 1500 ppm, 6 h/j, 5j/semaine, pendant 94 jours, n'induit aucune modification des paramètres spermatiques (nombre et concentration des spermatides dans les testicules, nombre de spermatozoïdes dans l'épididyme, mobilité ou morphologie spermatique).
-
Toxicité sur l’Homme
A faibles concentrations, la toxicité de l’acétate d’éthyle semble peu importante comparativement à celle de beaucoup de solvants industriels. Les effets irritants pour les muqueuses sont les plus communs. A fortes doses et particulièrement à température ambiante élevée, apparaissent des effets dépresseurs du système nerveux central.
Peu de données sont disponibles sur la toxicité humaine de l'acétate d'éthyle utilisé isolément, son usage étant le plus souvent associé à celui d'autres produits chimiques.
Toxicité aiguë [3, 18-21]
À la concentration de 400 ppm, l'acétate d'éthyle a des effets irritants pour les muqueuses nasale, pharyngo-laryngée et oculaire. Il est moins irritant que les acétates de propyle et de butyle, mais plus irritant que l'alcool éthylique. Une étude expérimentale chez 24 volontaires sains s'est intéressée aux effets d'une exposition à l'acétate d'éthyle à une concentration moyenne de 400 ppm pendant 4 heures (exposition continue stable ou pics d'exposition à 800 ppm) par rapport à une exposition à 2 ppm (témoin olfactif). L'intensité des symptômes sensoriels subjectifs augmentait de manière dose dépendante, sans différence significative entre l'exposition continue à 400 ppm et les pics d'exposition, sauf en ce qui concerne l'intensité de l'odeur perçue, plus importante en cas d'exposition continue. Les signes d'irritation (évalués sur la fréquence de clignements oculaires objectivée par électromyographie de l'orbiculaire des paupières et la mesure de la résistance nasale par rhinomanométrie antérieure active) ainsi que les tests neurocomportementaux n'étaient pas significativement différents.
Une atteinte collective a été rapportée en France dans un atelier de montage et de finition d'une fabrique de chaussures. Vingt-trois ouvriers sur 24 présentaient des lésions oculaires se manifestant soit par de simples irritations conjonctivales, soit dans la plupart des cas par une inflammation nettement caractérisée avec rougeur, larmoiement et œdème palpébral, réalisant une conjonctivite aiguë. Quelques-uns des sujets présentaient également de légères ulcérations de la cornée. Il n'a pas été noté de symptômes cutanés ou respiratoires associés et l'évolution a été favorable en quelques jours. L'enquête a pu éliminer différentes causes possibles et mettre en évidence la responsabilité d'un mélange contenant deux tiers d'acétate d'éthyle et un tiers d'acétate de n-butyle utilisé sur un poste de lustrage situé sous une buse de chauffage à air pulsé.
Les projections oculaires d'acétate d'éthyle peuvent entraîner une conjonctivite et parfois une kératite.
Le contact cutané prolongé avec l'acétate d'éthyle peut être responsable d'une dermatose irritative avec dessiccation de la peau. L'application cutanée d'une solution à 10 % sous pansement occlusif, pendant 48 heures, chez 25 sujets volontaires, n'a pas donné lieu à des réactions irritatives.
Lorsqu'ils sont inhalés à de très fortes concentrations, les esters aliphatiques simples sont dépresseurs du système nerveux central, provoquant céphalées, vertiges, asthénie, sensation d'ébriété et troubles de conscience. Le pouvoir narcotique de l'acétate d'éthyle est moindre que celui des acétates de butyle et de pentyle et des éthers, mais il est supérieur à celui de l'éthanol, de l'acétone ou d'alcanes comme le pentane.
Un cas de décès secondaire à l'effet narcotique du solvant ou à une anoxie a été rapporté en 1931 suite à l'inhalation de vapeurs d'une laque contenant 80 % d'acétate d'éthyle dans un espace confiné (intérieur d'un container). L'autopsie a révélé une hyperhémie des voies aériennes supérieures, des hémorragies pétéchiales de la plèvre et de l'épicarde, une hyperhémie de la rate et des reins et une gastrite hémorragique. Une odeur marquée d'acétate d'éthyle a été retrouvée au niveau de l'ensemble des organes examinés.
Toxicité chronique [3, 21, 22, 23]
Les esters aliphatiques saturés ne semblent pas exercer de toxicité cumulative systémique.
Cependant, il existe peu de données épidémiologiques sur la toxicité chronique de l'acétate d'éthyle.
Une irritation des yeux avec une hyperhémie de la conjonctive bulbaire sans anomalies cornéennes a été rapportée chez des ouvriers exposés de façon chronique à l'acétate d'éthyle à la concentration de 15 à 50 mg/L d'air associé à de l'acétate d'amyle.
Une dermite d'irritation (avec desquamation, rougeur et prurit) peut survenir après contact répété ou prolongé avec ce solvant. Des tests de sensibilisation effectués sur 25 sujets volontaires avec de l'acétate d'éthyle à 10 % dans la vaseline se sont révélés négatifs.
L'acétate d'éthyle participe probablement à la survenue du psychosyndrome organique dû aux solvants : irritabilité, troubles de la concentration, troubles du sommeil, troubles de la mémoire et baisse de l'efficience intellectuelle.
Effets génotoxiques [24-27]
Une étude comparant un groupe de 17 travailleurs dans 7 entreprises différentes de l'industrie de la peinture exposés à divers solvants organiques dont l'acétate d'éthyle (14 salariés exposés à une concentration de 1 à 129 mg/m3, avec une valeur moyenne de 20 mg/m3) à un groupe témoin n'a pas mis en évidence d'augmentation de la fréquence des échanges de chromatides sœurs dans les lymphocytes circulants.
Une évaluation des dommages à l’ADN par le test des comètes dans les lymphocytes périphériques n’a pas révélé de différence significative entre un groupe de 34 employées de 2 usines de fabrication de chaussures exposées à divers solvants organiques incluant l’acétate d’éthyle pour 18 d’entre elles (concentration de 400 ± 173,2 mg/m3 sur 8 heures dans le sous-groupe des salariées les plus exposées) et un groupe de témoins.
Une étude complémentaire réalisée chez un groupe élargi de 52 salariées des 2 mêmes usines a retrouvé une augmentation de la fréquence des micronoyaux, mais pas de celle des échanges de chromatides sœurs dans les lymphocytes circulants chez les exposés. On peut noter que la fréquence des micronoyaux chez les salariées de l’usine n’utilisant pas de l’acétate d’éthyle était moins importante, mais malgré tout significativement supérieure à celle chez les témoins. Les auteurs attribuaient les résultats à l’exposition au benzène contenu dans l’essence et au diisocyanate de diphénylméthane.
La fréquence des micronoyaux dans les cellules exfoliées de la muqueuse buccale était également plus élevée dans un groupe de 34 ouvriers de l’industrie de la chaussure exposés à des solvants organiques, dont l’acétate d’éthyle [concentration moyenne de 8,5 mg/m3 (0 - 261,9) sur 8 heures] et le toluène, par rapport au groupe témoin. Cependant, seule la concentration atmosphérique de toluène était corrélée à la fréquence des micronoyaux.
-
Interférences métaboliques
-
Cohérence des réponses biologiques chez l'homme et l'animal
