Pathologie - Toxicologie
-
Toxicocinétique - Métabolisme
La pyridine est bien absorbée par toutes les voies d’exposition. Elle est métabolisée partiellement par le foie et la forme inchangée ou les métabolites sont éliminés principalement dans l’urine; certains métabolites sont toxiques. Il n’y a pas d’accumulation dans l’organisme.
Chez l'animal
La pyridine est absorbée par le tractus gastro-intestinal, les poumons et la peau.
Elle est métabolisée de la même façon dans toutes les espèces étudiées, y compris l'homme (fig. 1) ; la quantité de chaque métabolite est fonction de l'espèce.
La pyridine est éliminée, sous forme inchangée ou métabolisée, en majorité par l'urine mais aussi par les fèces, la peau et les poumons. L'excrétion urinaire est biphasique, fonction de la dose et saturable : 24 heures après administration orale, le rat élimine 56 % d'une dose de 7 mg/kg et 20 % d'une dose de 357 mg/kg et le cobaye 76 % d'une dose de 7 mg/kg. Il ne semble pas y avoir d'accumulation tissulaire. Le métabolite principal, l'hydroxyde de N-méthylpyridinium, est excrété à raison de 20 à 40 % de la dose chez le chat, le cobaye, la gerboise, le lapin et le hamster et 5 à 12 % de la dose chez le rat, la souris et l'homme ; bien que l'urine soit la voie principale d'élimination, ce métabolite peut être formé et éliminé par les poumons. En exposition aiguë, il est plus toxique que la pyridine, mais moins toxique en exposition chronique.
Les métabolites produits par le métabolisme oxydatif, mis en évidence in vitro avec des microsomies de foie, de poumon et de rein humains et de rat, sont retrouvés dans l'urine après exposition in vivo. La 3-hydroxypyridine est présente surtout chez la souris et sous forme de traces chez le lapin, le pyridine N-oxyde chez le rat (10 % de la dose, injection intrapéritonéale), la souris et le cobaye (40 % de la dose, injection intrapéritonéale). Les 2- et 4-hydroxypyridine existent en quantités plus faibles dans les trois espèces.
Schéma métabolique
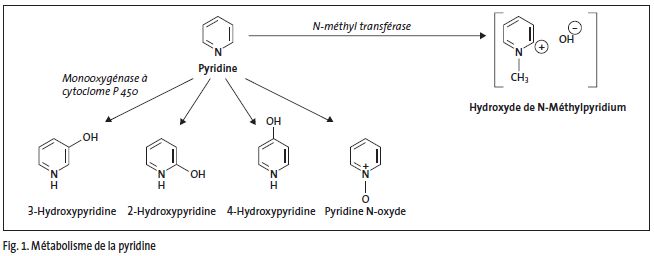
-
Mode d'actions
-
Toxicité expérimentale
Toxicité aiguë [1, 14]
Lors d’une exposition aiguë la pyridine entraîne des effets dépresseurs du système nerveux central et possède une action irritante sur la peau et les muqueuses.
Les effets majeurs de la pyridine, après exposition aiguë chez l'animal, sont une anesthésie et une irritation, quelle que soit la voie d'administration.
La DL50 orale est de 0,8 à 1,6 g/kg chez le rat et la souris et 4 g/kg chez le cobaye. La DL50 cutanée est de 1,12 g/kg chez le lapin et 1g/kg chez le cobaye. La CL50 est de 9000 ppm/1h chez le rat.
Administrée par voie orale (50 mg/kg), la pyridine induit, chez le rat, des effets hépatiques (dégénérescence graisseuse, engorgement vasculaire, hémorragie et nécrose) et un arrêt de la croissance pondérale. Le dépôt cutané de pyridine chez le lapin (0,5 - 1 et 2 g/kg) occasionne 100 % de létalité à la plus forte dose, une léthargie et une perte de poids sans effet macroscopique aux autres doses.
La pyridine est irritante pour la peau, l'œil et le tractus respiratoire. Au niveau oculaire, elle induit des lésions sévères avec opacification cornéenne non réversible et cicatrisation de la conjonctive. Déposée sur la peau (solution à 90 %), elle provoque nécrose, ulcération et régénération.
Elle n'est pas sensibilisante pour le cobaye.
Toxicité subchronique, chronique [15]
En cas d’exposition chronique, on observe une atteinte hépatique et rénale.
Après exposition chronique, les organes cibles de la pyridine sont le foie et les reins.
Administrée dans l'eau de boisson pendant 13 semaines chez le rat F344/N (5 - 10 - 25 - 55 - 90 mg/kg), la pyridine déclenche, aux deux plus fortes doses, une baisse de poids corporel et de la consommation hydrique, une anémie et des effets hépatiques dans les deux sexes (augmentation de poids, dégénérescence centrolobulaire, hypertrophie, inflammation chronique et pigmentation, augmentation de la concentration sérique en acide biliaire et des activités alanine aminotransférase et sorbitol déhydrogénase). À la plus forte dose, la durée du cycle œstral des femelles est allongée. Des effets rénaux (cylindres granuleux, gouttelettes hyalines, inflammation chronique, minéralisation et régénération) sont visibles uniquement chez les mâles à la plus forte dose et sont liés à une néphropathie à α2µ-globuline ; ils n'apparaissent pas chez le rat Wistar mâle dans les mêmes conditions.
Chez la souris, aux doses de 10-20-50-85 ou 160 mg/kg pour les souris mâles et de 10-20-60-100 ou 190 mg/kg pour les souris femelles dans l'eau de boisson pendant 13 semaines, on observe une baisse de poids chez les femelles, une diminution de la mobilité spermatique chez les mâles et, dans les deux sexes, une augmentation de poids du foie sans lésion histologique.
Les doses sans effet toxique observées (NOAEL) chez le rat et la souris sont respectivement de 25 et 20 mg/kg/j dans l'eau de boisson
Les lésions hépatiques et rénales sont plus sévères lorsque l'exposition dans l'eau de boisson est prolongée pendant 2 ans :
- chez le rat F344/N (7 - 14 - 33 mg/kg) : hépatocytomégalie centrolobulaire, vacuolisation cytoplasmique, fibrose périportale, dégénérescence et nécrose centrolobulaire, pigmentation sont observées à la plus forte dose dans le foie des animaux des deux sexes, hyperplasies, adénomes et carcinomes rénaux chez les mâles uniquement à la plus forte dose ;
- chez le rat Wistar mâle (8 - 17 - 36 mg/kg) : aux effets hépatiques identiques mais plus nombreux s'ajoutent une minéralisation de l'estomac glandulaire et une hyperplasie de la glande parathyroïde à toutes les doses. Ces animaux ne présentent pas de néoplasie rénale, mais une augmentation des adénomes testiculaires à la plus forte dose ;
- chez la souris B6C3F1 (35 - 65 - 110 mg/kg mâles et 15 - 3570 mg/kg femelles), les lésions hépatiques sont toutes néoplasiques (bénignes et malignes) et apparaissent dès la plus faible dose ; il n'y a pas d'autre lésion.
L'inhalation prolongée sur plusieurs mois de pyridine provoque, chez le rat, emphysème, bronchite chronique et dégénérescence graisseuse du foie et des reins.
Effets génotoxiques [16]
La grande majorité des tests réalisés in vitro et in vivo donnent des résultats négatifs.
In vitro
La pyridine n'est pas mutagène pour les souches TA98, TA100, TA1535 ou TA1537 de S. typhimurium ou les cellules L5178Y de lymphome de souris, avec ou sans activation métabolique. Elle n'induit pas d'échange entre chromatides sœurs ou d'aberration chromosomique dans les cellules ovariennes de hamster chinois en culture, avec ou sans activation métabolique. L’augmentation des échanges entre chromatides sœurs est rapportée dans une seule étude sur cellules de hamster, sans activation métabolique.
In vivo
Les résultats du test de mutation létale récessive liée au sexe chez la drosophile sont négatifs après administration orale et équivoques après injection. Il n'y a pas d'induction d'aberration chromosomique ou de micronoyau dans les cellules de la moelle osseuse de souris après injection intrapéritonéale (respectivement 600 et 500 mg/kg pc) ou par gavage (1000 mg/kg pc).
Effets cancérogènes [15, 16]
Chez le rat et la souris, la pyridine induit des tumeurs bénignes et malignes dans plusieurs organes (foie, reins, sang et testicules).
Des rats (F344/N et Wistar) et des souris (B6C3F1) des 2 sexes ont été exposés à la pyridine via l'eau de boisson pendant 2 ans. Les doses correspondantes étaient les suivantes :
- 0-35-65-110 mg/kg pc/j pour les souris mâles et 0-15-35-70 mg/kg pc/j pour les souris femelles,
- 0-7-14-33 mg/kg pc/j pour les rats F344/N mâles et femelles, et 0-8-17-36 mg/kg pc/j pour les rats Wistar mâles.
Les souris des deux sexes présentent une augmentation de l’incidence des néoplasmes hépatocellulaires de type adénomes, carcinomes et hépatoblastomes ; de nombreux animaux développent des néoplasmes multiples.
Chez les rat F344/N mâles, la pyridine augmente l’incidence des adénomes et des adénocarcinomes dans les tubes rénaux à la plus forte dose testée soit 33 mg/kg pc/j ; chez la femelle, elle augmente l'incidence des leucémies à cellules mononucléaires à partir de 14 mg/kg/j.
Chez le rat Wistar mâle, une augmentation de l’incidence des adénomes des cellules interstitielles testiculaires est rapportée à la plus forte dose testée soit 36 mg/kg pc/j.
A partir de ces données, le CIRC a classé la pyridine dans le groupe 2B, cancérogène possible pour l’Homme.
Mode d'action
Chez le rat, la pyridine est un inducteur des cytochromes P450 (CYP1A1 dans les reins, le poumon, le foie et les lymphocytes, CYP1A2 dans le foie, CYP2E1 dans le foie et les testicules) et de l'hème oxygénase dans le poumon et le foie. Les inducteurs enzymatiques sont souvent des cancérogènes épigénétiques et provoquent le développement de tumeurs du foie et/ou de la thyroïde.
Effets sur la reproduction
Très peu de données sont disponibles concernant les effets sur la reproduction et le développement de la pyridine ; des modifications du cycle œstral et de la motilité spermatique ont été rapportés lors d'études chroniques.
Même si aucune étude de reprotoxicité n'a été réalisée, les études chroniques (13 semaines) réalisées chez le rat et la souris ont mis en évidence une augmentation de la durée du cycle oestral (rats femelles à la plus forte dose, 90 mg/kg/j) et une diminution de la mobilité spermatique (souris mâles, dès 50 mg/kg/j).
-
Toxicité sur l’Homme
La pyridine provoque essentiellement des effets sur le système nerveux central et le tractus gastro-intestinal. Elle est irritante pour la peau ou les muqueuses. Des atteintes hépatiques ont été rapportées après expositions répétées.
Toxicité aiguë [1, 17-20]
En milieu professionnel, la pyridine peut pénétrer dans l'organisme, principalement par contact cutané ou par voie respiratoire, et plus rarement par voie orale.
Les deux principaux organes cibles sont le système nerveux central et le tractus gastro-intestinal. Quelle que soit la voie d'intoxication, les signes neurologiques dominent le tableau, associant céphalées, vertiges, asthénie, nervosité, confusion ; ils peuvent être associés à des signes digestifs tels que nausées, anorexie, vomissements, voire diarrhées.
Par inhalation, les vapeurs de pyridine sont irritantes pour les muqueuses oculaires, nasales et respiratoires.
La pyridine par contact cutané ou par projection provoque une irritation de la peau et des muqueuses, voire des brûlures.
La pyridine a été à l'origine de quelques cas de sensibilisation cutanée à type d'eczéma.
Toxicité chronique [1, 19, 20]
Lors d'expositions chroniques à des vapeurs de pyridine, des symptômes neurologiques et digestifs (tels qu'anorexie, nausées, céphalées, asthénie, insomnie, nervosité, voire des douleurs lombaires ou abdominales basses avec pollakiurie) peuvent apparaître à partir de 6 ppm ; ces symptômes sont le plus souvent transitoires.
Les autres atteintes décrites lors d'ingestions médicamenteuses répétées sont une atteinte hépatique (dégénérescence graisseuse, infiltration cellulaire, voire cirrhose ou destruction parenchymateuse en cas d'intoxication sévère) ou plus rarement rénale.
-
Interférences métaboliques
-
Cohérence des réponses biologiques chez l'homme et l'animal
