Pathologie - Toxicologie
-
Toxicocinétique - Métabolisme [2, 12, 13]
Le 1,3-butadiène pénètre dans l’organisme principalement par le tractus respiratoire. Il s’y distribue largement et est éliminé, sous forme de CO2, dans l’air expiré et, sous forme conjuguée, dans les urines.
Chez l'animal
Absorption
Le gaz pénètre, par diffusion passive, des alvéoles vers le sang ; la quantité relative absorbée diminue quand la concentration augmente (1,5 % de 7 100 ppm et 17 % de 0,8 ppm chez le rat, 4 % de 1 000 ppm et 20 % de 7 ppm chez la souris, lors d'une exposition pendant 6 heures). La quantité totale retenue par kilogramme de poids est 4 à 7 fois plus importante chez la souris que chez le rat. L'absorption du 1,3-butadiène est beaucoup plus faible chez les primates et l'homme.
Distribution
Le 14C]-1,3-butadiène inhalé se distribue largement dans les tissus du rat et de la souris, dès le début de l'exposition. Les concentrations les plus fortes, 1 heure après la fin de l'exposition, sont retrouvées dans le sang, le tractus respiratoire, les intestins, le foie, les reins, la vessie et le pancréas ; les tissus de la souris contiennent des concentrations plus importantes que ceux du rat. Dans les érythrocytes, le 1,3-butadiène et ses métabolites époxydes forment des adduits avec l'hémoglobine, dont la quantité est fonction de la dose inhalée ; leur durée de vie est de 24 à 65 jours chez le rat et la souris. Le taux d'adduits formés, respectivement chez la souris, le rat et l'homme, est de 0,5, 0,2 et 0,004 pmoles/g d'hémoglobine/ppm-h.
Métabolisme
Selon les données obtenues in vitro et in vivo, la transformation métabolique du 1,3-butadiène est identique pour toutes les espèces étudiées, y compris l'homme (fig. 1) ; cependant, des différences d'absorption et de cinétique métabolique entre les espèces modifient les concentrations sanguines et la charge corporelle en 1,3-butadiène et en ses métabolites. Le taux de formation de l'époxybutène est inversement proportionnel à l'activité époxyde hydrolase hépatique de chaque espèce : la charge corporelle en époxybutène chez la souris est 4 fois plus importante que chez le rat et 100 fois plus importante que chez le singe et l'homme. L'époxybutène est oxydé en diépoxybutane, principalement chez la souris, 40 à 160 fois plus que chez le rat ; chez l'homme, la formation de diépoxybutane n'est pas décelable. Chez le rat, la concentration sanguine et tissulaire d'époxybutène ne varie pas selon le sexe, en revanche, le taux de diépoxybutane est plus important chez les femelles que chez les mâles.
Les différents époxydes ainsi obtenus peuvent alors :
- soit être inactivés par hydrolyse ;
- soit former des acides mercapturiques tels que l'acide dihydroxybutylmercapturique (DHBMA) et l'acide monohydroxy-3-buténylmercapturique (MHMBA) ;
- soit former des liaisons covalentes avec l'ADN (mono- et di-époxy) ainsi qu'avec des protéines comme l'hémoglobine.
Dans les érythrocytes, il se forme des adduits à l'hémoglobine. Ainsi, les N-(1- et N-(2-hydroxy-3-butényl)valine (MHbVal) ainsi que le N-(2,3,4-trihydroxybutyl)valine (THbVal), provenant respectivement de la réaction de l'époxybutène et de l'époxybutanediol avec la partie N-terminale de la valine de l'hémoglobine, ont été identifiés chez des travailleurs exposés au 1,3-butadiène à des concentrations inférieures au ppm [17, 19, 20, 23].
Schéma métabolique
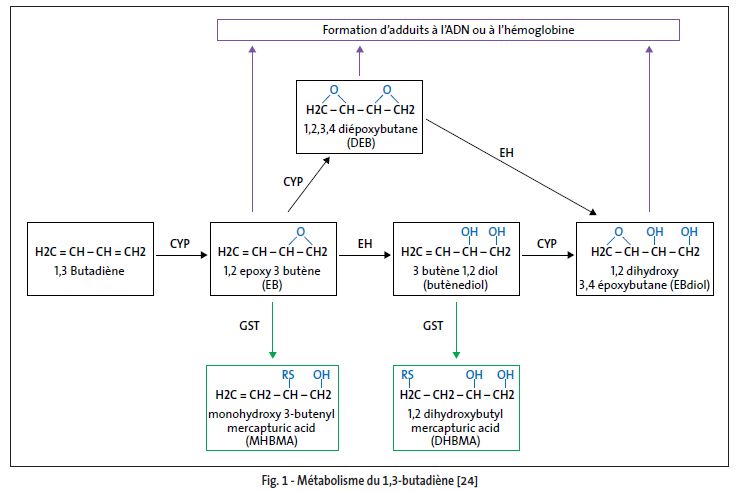
Excrétion
Le 1,3-butadiène est éliminé essentiellement par l'air expiré sous forme de CO2 ,ainsi que dans les urines sous forme de 2 métabolites principaux :
I) 1,2-dihydroxy-4-(N-acétyl-cystéinyl)-butane, formé à partir du conjugué au glutathion du 3-butène-1,2-diol
II) S-(1-hydroxy-3-butén-2-yl)-N-acétylcystéine, formée à partir du conjugué au glutathion de l'époxybutène ;
et 4 autres métabolites urinaires non identifiés. Le taux d'excrétion des métabolites (I : II) est (20 % : 80 %) chez la souris, (52 % : 48 %) chez le rat, (90 % : 10 %) chez le singe et (> 97 % : < 3 %) chez l'homme.
Le styrène inhibe le métabolisme du 1,3-butadiène pour des concentrations inférieures à 90 ppm de 1,3-butadiène uniquement ; ce qui prouverait l'implication de 2 mono-oxygénases à cytochrome P450 différentes (2E1 et 3A4) dans le métabolisme du 1,3-butadiène, dont une seule serait inhibée par le styrène.
Surveillance Biologique de l'exposition
Les dosages des acides mercapturiques, acide dihydroxybutylmercapturique (DHBMA) et acide monohydroxy-3-butényl mercapturique (MHBMA), dans les urines de fin de poste et fin de semaine de travail, est proposé pour la surveillance biologique de l’exposition au 1,3-butadiène. Ces indicateurs sont bien corrélés avec l'exposition de la journée, une accumulation étant observée au cours de la semaine de travail.
L'Anses a considéré qu'aucune valeur limite biologique (VLB) ne pouvait être proposée pour ces indicateurs puisque les valeurs calculées à partir des corrélations avec les concentrations atmosphériques en 1,3-butadiène (0,08 mg/m3, 0,008 mg/m3, 0,0008 mg/m3) associées aux trois niveaux de risque additionnel de décès par leucémie (10-4, 10-5, 10-6) seraient extrapolées pour des concentrations atmosphériques très basses par rapport à celles ayant permis d'établir ces corrélations. De plus, elles sont très proches voire inférieures aux valeurs retrouvées en population générale. Des valeurs biologiques d’interprétation (VBI) professionnelles ont été établies par d’autres organismes.
Des valeurs VBI issues de la population générale ont été recommandées par l’Anses (pour le DHBMA et le 3-MHBMA, principal isomère du MHBMA, en fonction du statut tabagique) et par la Commission allemande DFG (pour le DHBMA et le MHBMA, chez les non-fumeurs).
Les adduits à l’hémoglobine MHBVal et THBVal reflètent l’exposition des 4 mois précédents. Aucune VBI n’a été proposée par l’ANSES pour ces indicateurs : pas de VLB pour les mêmes raisons que celles évoquées pour le dosage des acides mercapturiques ; pas de VBI issue de la population générale, en raison de données insuffisantes.
Une valeur BEI pour le MHBVal de 2,5 pmol/g Hb après au moins 4 mois d'exposition a été établie par l’ACGIH, correspondant à une exposition atmosphérique à 2 ppm (4,4 mg/m3) de 1,3-butadiène.
-
Mode d'actions
-
Toxicité expérimentale
Toxicité aiguë [2, 12]
Le 1,3-butadiène est faiblement toxique en exposition aiguë. L’organe cible, à fortes concentrations, est le système nerveux central.
La DL50 orale est 5 480 mg/kg chez le rat et 3 210 mg/kg chez la souris. La CL50 est de 270 mg/L ou 122 000 ppm/ 2h chez la souris et 285 mg/L ou 129 000 ppm/4h chez le rat.
L'exposition, à fortes concentrations, de lapins (250 000 ppm, 8 à 10 mn), de souris (200 000 ppm, 6 à 10 mn) ou de rats (129 000 ppm, 1 h) induit une anesthésie profonde et la mort par paralysie respiratoire. Chez le lapin exposé à 90 000 ppm pendant 2 heures, on observe un effet hématologique (leucocytose, neutrophilie, lymphopénie et monocytose).
Une baisse significative de la teneur en glutathion (10 à 95 % selon la concentration inhalée) est observée dans les poumons, le foie et le cœur du rat et de la souris ; cette réduction est liée au taux de métabolites époxydes formés, elle est plus importante dans les poumons de la souris que dans ceux du rat et semblable dans le foie des deux espèces.
Une exposition aiguë au 1,3-butadiène par inhalation provoque une conjonctivite chez la souris (90 000 - 140 000 ppm) et le lapin (150 000 - 250 000 ppm). Il n'existe pas de données sur le potentiel irritant du 1,3-butadiène pour la peau ; cependant, au vu du faible point d'ébullition, l'exposition au liquide pourrait engendrer des lésions tissulaires.
Toxicité subchronique, chronique [2, 12, 15]
Le 1,3-butadiène, en exposition répétée, induit, chez la souris, des lésions prolifératives dans le cœur, les poumons et l’estomac, ainsi qu’une atrophie testiculaire et ovarienne et un effet sur la moelle osseuse. Chez le rat, les effets observés sont minimes.
Il existe une nette différence de toxicité du 1,3-butadiène après exposition répétée entre le rat et la souris. Le 1,3-butadiène est faiblement toxique pour le rat, des effets minimes sont observés après exposition à 8 000 ppm pendant 2 ans (légère incoordination et faiblesse des membres, augmentation de poids du foie, des reins, du cœur, des poumons et de la rate avec néphrose et métaplasie focale des poumons).
Au contraire, le 1,3-butadiène est très toxique pour la souris induisant :
- une létalité accrue et un développement tumoral à partir de 20 ppm ;
- une perte de poids corporel, une hyperplasie de l'endothélium cardiaque, de l'épithélium des alvéoles et du préestomac, et des papillomes à cellules squameuses du pré-estomac et de la glande lacrymale à partir de 625 ppm, 6 h/j, 5 j/sem., 60 semaines ;
- une atrophie gonadique (testicules et ovaires) chez le mâle exposé à 625 ppm et chez la femelle exposée à 6,25 ppm. Les effets sur l'ovaire seraient dus au diépoxybutane, métabolite du 1,3-butadiène et à la baisse en glutathion ;
- une altération de la moelle osseuse qui se traduit par une anémie macrocytaire mégaloblastique, une leucopénie, une modification du développement des cellules souches hématopoïétiques à partir de 1 250 ppm, 6 h/j, 5 j/sem., 6 semaines ;
- des modifications de la rate (augmentation de l'hyperplasie érythroïde, hématopoïèse extramédullaire et légère baisse du nombre de cellules) et du thymus (baisse du nombre de lymphocytes corticaux) à 1 250 ppm pendant 24 semaines, sans effet toxique persistant sur le système immunologique [15].
Le 1,3-butadiène a une faible toxicité pour le cobaye, le lapin et le chien en exposition répétée (0 - 600 - 2 300 - 6 700 ppm, 7,5 h/j, 6 j/sem., 8 mois).
Effets génotoxiques [2, 12, 15-19]
Le 1,3-butadiène est faiblement génotoxique in vitro, en présence d’activation métabolique, et génotoxique in vivo, pour la souris. Le potentiel génotoxique est lié à la formation, in vitro et in vivo, de métabolites époxydes réactifs, 1,2-époxy-3-butène et 1,2:3,4-diépoxybutane.
In vitro, le 1,3-butadiène est mutagène pour Salmonella typhimurium TA1530 et TA1535 dans le test d'Ames en présence d'activateur métabolique. Dans les cellules de mammifères, des résultats positifs ont été obtenus, en présence d'activateur métabolique, sur les cellules de lymphome de souris ; le test d'induction d'échanges entre chromatides-sœurs donne des résultats contradictoires : négatifs sur cellules ovariennes de hamster chinois (CHO) et positifs sur lymphocytes humains [16].
Dans ces cellules, après un traitement de 2 heures, le 1,3- butadiène produit une augmentation faible mais reproductible des échanges entre chromatides-sœurs, avec et sans activation métabolique ; les 2 époxydes sont fortement inducteurs sans activation métabolique. La concentration effective la plus basse est : 2 000 µM de butadiène, 25 µM d'époxybutène, et 0,5 µM de diépoxybutane [17].
In vivo, il induit :
- des alkylations, cassures simple brin, adduits et lésions de l'ADN chez la souris ; chez le rat, seules des cassures simple brin dans le foie et des adduits ont été montrés ;
- des mutations géniques dans les poumons des souris transgéniques (62,5 ppm, 6 h/j, 5 j/sem., 4 semaines) et les splénocytes des souris de souche normale ;
- des micronoyaux dans la moelle osseuse, le sang périphérique (à partir de 50 ppm, 6 h/j, 5 jours) et les sperma- tides (à partir de 200 ppm, 6 h/j, 5 jours) chez la souris, mais ni chez le rat ni chez le hamster[18] ;
- des aberrations chromosomiques (625 ppm, 6 h/j, 10 jours ou 1 250 ppm, 96 heures) et des échanges entre chromatides sœurs (6,25 ppm, 6 h/j, 10 jours) dans la moelle osseuse de souris [19];
- des mutations létales dominantes sur les cellules germinales de souris (1 250 ppm, 6 h/j, 5 j/sem., 10 semaines) qui mènent à une augmentation du taux de perte embryonnaire postimplantatoire ; il n'y a pas d'effet chez le rat.
Les époxydes sont génotoxiques, in vitro dans de nombreux tests et, in vivo, sur les cellules somatiques et germinales du rat et de la souris et les cellules somatiques du hamster.
Effets cancérogènes [2, 12, 20, 21]
Le 1,3-butadiène est cancérogène pour le rat et la souris ; cette dernière est beaucoup plus sensible et présente un nombre de sites tumoraux beaucoup plus important.
Il y a de grandes différences d'espèce dans le potentiel cancérogène et le spectre des tumeurs.
La souris développe des tumeurs à faible concentration avec une exposition longue (à partir de 6,25 ppm, 6 h/j, 5 j/sem., 104 semaines) ou à forte concentration pendant un temps d'exposition court (625 ppm, 6 h/j, 5 j/sem., 13 semaines) [20] :
- chez la femelle : carcinomes mammaires (62,5 ppm), néoplasmes de l'ovaire (62,5 ppm), néoplasmes hépatocellulaires (20 ppm) ;
- dans les 2 sexes : hémangiosarcomes du cœur (200 ppm femelles, 62,5 ppm mâles), lymphomes malins (200 ppm femelles, 625 ppm mâles), néoplasmes alvéolo-bronchiolaires (6,25 ppm femelles et 62,5 mâles), néoplasmes à cellules squameuses du préestomac (625 ppm femelles, 200 ppm mâles).
Le rat développe des tumeurs à partir de 1 000 ppm, 6 h/j, 5 j/sem., 105 - 111 semaines [21] :
- chez la femelle : adénomes et carcinomes mammaires, adénomes des cellules folliculaires de la thyroïde ;
- chez le mâle : tumeurs testiculaires des cellules de Leydig.
La différence de sensibilité d'espèce pourrait être liée à une différence de métabolisme mais n'est pas clairement explicitée.
Effets sur la reproduction [2]
Les études chez le cobaye, le lapin, le rat (jusqu’à 6 700 ppm pendant 8 mois) et la souris (jusqu’à 1 300 ppm pendant 5 jours) n’ont pas montré d’effet toxique du 1,3-butadiène sur la fertilité.
En revanche, il induit, à des concentrations toxiques pour les mères, un retard du développement fœtal chez le rat et la souris.Chez la souris, une augmentation légère des pertes post-implantatoires a été observée uniquement dans les deux premières semaines après exposition courte (tests de létalité dominante, 1 000 ppm, 6 h/j, 5 j) ; lors d'expositions prolongées, le 1,3-butadiène provoque une atrophie gonadique. Chez le rat, des tumeurs testiculaires ont été montrées à partir de 1 000 ppm.
Des rates exposées à 0 - 200 - 1 000 - 8 000 ppm, 6 h/j du 6ième au 15ième jour de gestation, présentent une baisse de la prise de poids à partir de 1 000 ppm ; après exposition à 8000 ppm, la croissance et le poids fœtal diminuent, la mortalité postimplantatoire ainsi que le taux de côtes malformées, d'opacité oculaire et de défauts sévères du squelette sont augmentés. Chez la souris (0 - 40 - 200 - 1 000 ppm, 6 h/j, du 6ième au 15ième jour de gestation), le 1,3- butadiène induit, en absence de toxicité maternelle, une baisse de poids fœtal (40 ppm) ; des anomalies fœtales, vertèbres supplémentaires et ossification réduite des sternèbres, sont observées à des concentrations toxiques pour les mères (à partir de 200 ppm).
-
Toxicité sur l’Homme
L’exposition aiguë par inhalation massive de gaz peut provoquer des irritations respiratoires, oculaires, et des signes neurologiques non spécifiques, pouvant aller jusqu’au coma. Le contact cutané avec le gaz peut entrainer des brulures par le froid. Il n’existe pas de données sur l’exposition répétée isolée au 1,3-butadiène. Les données sur d'éventuels effets génotoxiques sont contradictoires. Une association entre le niveau d’exposition et le risque de mortalité par leucémie est décrite dans l’industrie du styrène-butadiène. Dans l’industrie du 1,3-butadiène monomère, une augmentation significative de la mortalité due aux cancers lymphatiques et hématopoïétiques a été rapportée. Aucune donnée sur la reprotoxicité n’est disponible chez l’homme.
Ce sont principalement les effets cancérogènes chez l'homme qui ont été étudiés lors d'expositions professionnelles. Les autres aspects de la toxicologie humaine ont par contre fait l'objet de peu de publications.
Toxicité aiguë [2, 24]
Les intoxications peuvent faire suite à une inhalation massive du gaz ou une projection de celui-ci sur la peau. Après inhalation de concentrations supérieures à 10 000 ppm, les sujets présentent une toux, une ébriété et une sensation de fatigue ; ces signes peuvent s'accompagner de céphalées et d'un flou visuel. À plus forte concentration, on peut observer un coma. Le gaz est moyennement irritant pour les yeux, la gorge et les voies aériennes supérieures ; cet effet a notamment été observé chez des volontaires exposés à une concentration de 2 000 ppm pendant 7 heures.
Si le butadiène semble peu irritant pour la peau, le contact avec le gaz peut entraîner des lésions de brûlures par le froid.
Toxicité chronique [2, 22, 23]
Il n'existe pas de données mentionnant des effets liés à une exposition chronique isolée à cette substance. Au cours d'une enquête de suivi d'employés d'une entreprise de caoutchouc, un excès de diabètes et de maladies ischémiques cardiaques a été constaté. Ces sujets avaient été exposés à de nombreux produits, dont le 1,3-butadiène.
Plusieurs études ne rapportent pas de lien entre exposition au 1,3-butadiène et développement d'anomalies hématologiques chez des sujets professionnellement exposés à des concentrations moyennes allant de 0,25 ppm jusque 4,55 ppm tandis qu'une étude rapporte une augmentation des lymphocytes et des plaquettes chez des sujets exposés au 1,3-butadiène à des concentrations de l'ordre de 2 ppm.
Des effets neurotoxiques sont rapportés par certains auteurs (sans relation dose-effet déterminée).
Effets génotoxiques [17, 19, 20, 23]
Les résultats d'études épidémiologiques sur les effets génotoxiques chez l'homme du 1,3-butadiène sont contradictoires. Plusieurs auteurs ne retrouvent pas d'association entre les marqueurs d'effets génotoxiques (mutations HPRT sur lymphocytes sanguins, aberrations chromosomiques) chez les travailleurs et l'exposition au butadiène à des concentrations inférieures à 1 ppm sur 8 heures/jour ou de 2 ppm sur 6 heures/jour ; d'autres auteurs rapportent chez des travailleurs exposés au butadiène une augmentation significative des délétions du gène HPRT des lymphocytes sanguins (concentrations moyennes de butadiène supérieures à 3 ppm) et une seule étude récente montre une augmentation des micronoyaux sur des lymphocytes de sujets fortement exposés au 1,3-butadiène en Chine (mais les co-expositions ne peuvent être exclues).
Effets cancérogènes [2, 24-26]
Le potentiel cancérogène du 1,3-butadiène chez l'homme a principalement été évalué à partir d'études réalisées chez les travailleurs de l'industrie du caoutchouc synthétique (2 cohortes) ou utilisant du butadiène monomère (3 cohortes). Ces études épidémiologiques ont permis d'établir un lien de causalité entre l'apparition de leucémies et de lymphomes non-hodgkiniens et l'exposition des travailleurs au 1,3-butadiène [22, 24].
Dans l'industrie du caoutchouc synthétique (production de polymères styrène-butadiène), la plus large étude concerne 17 000 travailleurs issus de 8 unités de fabrication aux Etats-Unis et au Canada (« cohorte Delzell »). Une relation dose-réponse significative entre l'exposition cumulée au 1,3-butadiène et la mortalité par leucémie (leucémies myéloïdes chronique et lymphoïdes chroniques) est retrouvée ; cet excès de décès est noté chez les sujets les plus fortement exposés et dont la durée d'exposition est la plus longue (> 10 ans). Cette relation est indépendante des expositions concomitantes au styrène, au benzène et au diméthyldithiocarbamate.
Dans l'industrie du butadiène monomère aux Etats-Unis (« cohorte Divine »), une cohorte de 2 800 travailleurs actualisée à plusieurs reprises (1990, 1993, 1996 et 2001) a été analysée : un léger excès de risque statistiquement significatif de décès par cancers lymphatiques et hématopoïétiques (lymphomes non hodgkiniens, leucémies) est observé parmi les ouvriers recrutés avant 1950 (une relation dose-réponse n'a pu être mise en évidence probablement en raison du faible effectif de la cohorte) ; des excès de décès par lymphosarcomes et réticulosarcomes sont également notés dans cette cohorte.
Les données disponibles sur la cancérogénicité du 1,3-butadiène sont suffisantes pour dériver une relation dose-effet aux faibles doses et leur associer des excès de risque sur lesquels s'appuyer pour proposer une VLEP-8h [22].
Effets sur la reproduction
On ne dispose d'aucune donnée sur ce produit concernant les effets sur la reproduction chez l'homme.
-
Interférences métaboliques
-
Cohérence des réponses biologiques chez l'homme et l'animal
