Pathologie - Toxicologie
-
Toxicocinétique - Métabolisme [1, 10]
Le naphtalène, après absorption, est oxydé par l’organisme et éliminé dans les urines sous forme de plusieurs métabolites dont le 1-naphtol qui est en relation, chez l’homme, avec la concentration en naphtalène inhalé.
Chez l'animal
Absorption
Chez le rat, le naphtalène est bien absorbé par le tractus gastro-intestinal ; la forte solubilité de la substance dans les lipides suggère une absorption cutanée non négligeable.
Distribution
Après absorption, le naphtalène ou ses métabolites sont distribués, par le sang, dans tout l’organisme. Après une exposition par voie orale chez le poulet, le porc et la vache, les concentrations les plus élevées sont mesurées au niveau du tissu adipeux, des poumons, du foie, du cœur et de la rate. Aucune donnée comparable n’est disponible chez les rongeurs.
Métabolisme
Le métabolisme du naphtalène a été étudié in vitro et in vivo chez l’animal (voir fig. 1). La première phase, catalysée par les mono-oxygénases à cytochrome P450, est une oxydation produisant un époxyde électrophile intermédiaire. Cette phase se déroule dans le foie mais aussi dans d’autres tissus comme les yeux ou le poumon. Elle est suivie soit d’une hydratation et d’une réduction qui aboutit à la formation de naphtoquinones, soit d’un réarrangement en naphtols qui sont conjugués ou hydratés en naphtoquinones, soit d’une conjugaison avec le glutathion et la cystéine en dérivés mercapturiques.
Schéma métabolique
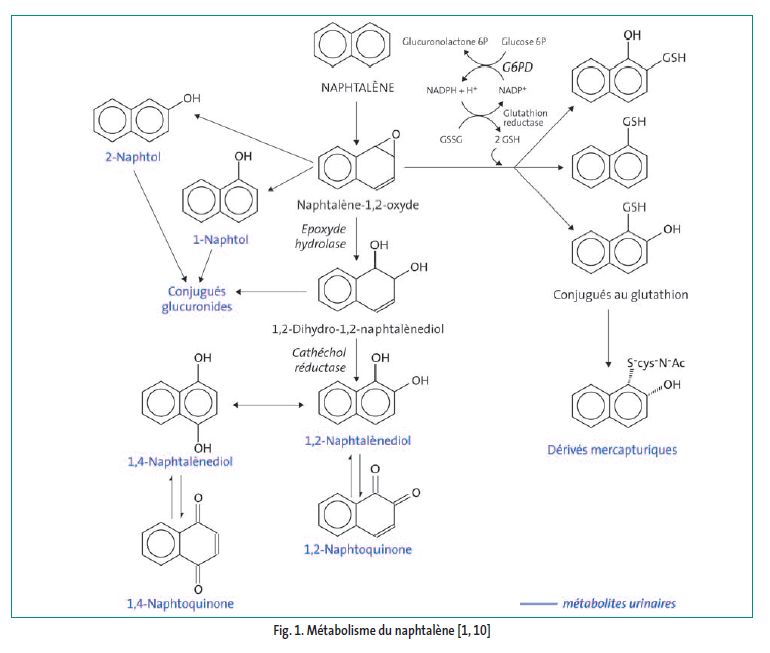
Excrétion
Le métabolisme est extensif et l’élimination rapide, essentiellement par voie rénale après circulation entéro-hépatique. Chez le rat, 72 heures après exposition orale à du 14C-naphtalène, 83 % des molécules marquées sont éliminés dans l’urine, 6 % dans les fèces et 4 % restent dans la carcasse. Dans les métabolites urinaires identifiés, on note 38,1 % de dérivés mercapturiques, 23,9 % de 1,2-dihydro-1,2-naphtalènediol glucuronide, 4,9 % de 1,2- naphtalènediol, 4,6 % de naphtols et naphtol glucuronides; le 1,2-dihydro-1-hydroxy-2-méthylthionaphtalène glucuronide (4,6 %) a été identifié, chez le rat, comme métabolite provenant de la transformation du naphtalène par la flore intestinale.
-
Mode d'actions
L’effet hémolytique du naphtalène est potentialisé, chez l’homme, par un déficit en glucose-6-phosphate dés- hydrogénase (G6PD), enzyme anti-oxydante, qui sert à maintenir une concentration suffisante de glutathion réduit (GSH) indispensable pour assurer l’intégrité de la membrane des érythrocytes. Les sujets souffrant d’un déficit en G6PD parviennent néanmoins à maintenir un taux suffisant de GSH et ne présentent pas spontanément d’accès d’hémolyse. Plusieurs hypothèses peuvent être avancées pour expliquer l’impact du naphtalène sur la séquence d’événements décrite figure 1 : déficit de glutathion créé par la conjugaison du glutathion avec le naphtalène (d’où une vulnérabilité de la cellule à l’oxydation), métabolites du naphtalène agissant comme des inhibiteurs de la glutathion peroxydase ou de la glutathion réductase ou action directe du glutathion ou de ses métabolites comme agent oxydant.
-
Toxicité expérimentale
Toxicité aiguë [1, 10, 11]
La toxicité aiguë du naphtalène est modérée par voie orale. Il est peu ou pas irritant.
Voie
Espèce
DL50/CL50
Inhalatoire
Rat
> 0,5 mg/L/8 h
Orale
Rat
1110-2400 mg/kg
Souris
354-710 mg/kg
Cobaye
1200 mg/kg
Cutanée
Rat
> 2 500 mg/kg
Lapin
> 2 000 mg/kg
Tableau 1. Toxicité aiguë du naphtalène
Après exposition par voie orale, les symptômes observés sont :
- chez le rat, des diarrhées;
- chez la souris, une baisse de la fréquence respiratoire et une ataxie ;
- chez le chien (1500 mg/kg), une léthargie, des vomissements et des diarrhées avec baisse du taux d’hémoglobine, présence de corps de Heinz dans les globules rouges et réticulocytose à partir du 7e jour.
Aucun effet n’est montré par voie cutanée ou inhalatoire. Quelques études par voie intrapéritonéale montrent un effet toxique pour le tractus respiratoire: nécrose et exfoliation de l’épithélium olfactif nasal chez le rat (> 200 mg/kg), vacuolisation, exfoliation et nécrose des cellules de Clara (≥ 50 mg/kg), des cellules des bronchioles terminales (≥ 100 mg/kg), de la trachée et des bronches (≥ 300 mg/kg) et de l’épithélium nasal (≥ 400 mg/kg) chez la souris. Chez le hamster, on note une vacuolisation des cellules bronchiques et une nécrose de l’épithélium nasal (≥ 400 mg/kg) mais pas d’effet sur la trachée.
Le naphtalène est faiblement irritant pour la peau du lapin (érythème et œdème légers avec une réversibilité complète en 6 jours) et non irritant pour les yeux. Il n’est pas sensibilisant pour le cobaye.
Toxicité subchronique, chronique [1, 10]
Une exposition répétée ou prolongée induit des réponses différentes selon les espèces: irritation, cataracte ou anémie hémolytique.
Les animaux répondent différemment selon l’espèce à une exposition au naphtalène. La souris est plus sensible que le rat ou le lapin (100 % de mortalité à 500 mg/kg/j pendant 8 jours) ; la NOAEL pour les effets systémiques est de 133 mg/kg/j pour une exposition de la souris par voie orale pendant 90 jours.
Une anémie hémolytique est notée chez le chien après une exposition orale à 220 mg/kg/j pendant 7 jours mais pas chez les rongeurs même après une exposition prolongée de 2 ans.
La formation de cataracte est l’effet principal observé chez le rat et le lapin après exposition orale à 700 et 1000 mg/kg/j respectivement pendant 10 à 180 jours, mais cet effet n’est pas observé chez la souris. Le métabolite responsable de l’opacité du cristallin serait la 1,2-naphtoquinone.
Une inflammation de l’épithélium olfactif nasal est induite après inhalation à des concentrations égales ou supérieures à 10 mg/m3 pendant 90 jours chez le rat; chez la souris, l’inflammation (≥ 50 mg/m3) s’étend aux poumons (adénomes broncho-alvéolaires bénins, ≥ 150 mg/m3 pendant 104 sem.).
Par voie cutanée, la NOAEL est supérieure à 1000 mg/kg/j chez le rat exposé 6 h/j, 5 j/sem. pendant 90 jours.
Effets génotoxiques [1, 10]
Le naphtalène n’induit pas de génotoxicité in vitro et in vivo dans les tests pratiqués.
In vitro, il n’est pas mutagène pour les bactéries et n’augmente pas la synthèse non programmée de l’ADN dans les hépatocytes de rat ; il est clastogène pour les cellules ovariennes de hamster chinois, en présence d’activateurs métaboliques uniquement, mais n’induit pas d’échanges entre chromatides sœurs dans ces mêmes cellules ou dans les lymphocytes humains.
Les tests pratiqués in vivo donnent également des résultats négatifs (micronoyau dans la moëlle osseuse de souris 250 mg/kg - voie intrapéritonéale; synthèse non programmée de l’ADN dans le foie de rat, 600 - 1600 mg/kg - voie orale).
Effets cancérogènes [1, 10]
Le naphtalène est cancérogène pour le rat au niveau des localisations de l’inflammation déclenchée par l’inhalation.
Le naphtalène donne des résultats négatifs dans les tests de transformation cellulaire in vitro (cellules embryonnaires de hamster syrien, fibroblastes pulmonaires humains).
Chez le rat (0 - 10 - 30 - 60 ppm, 6 h/j, 5 j/sem. pendant 105 semaines), il induit des tumeurs du tractus respiratoire en conséquence de modifications inflammatoires: neuroblastomes de l’épithélium olfactif nasal (≥ 10 ppm mâle, ≥ 30 ppm femelle), adénomes de l’épithélium respiratoire nasal (≥ 30 ppm mâle, ≥ 10 ppm femelle) mais pas de tumeur pulmonaire. La souris (0-10-30 ppm, 6 h/j, 5 j/sem. pendant 105 semaines) présente une augmentation, significative chez les femelles, des adénomes broncho-alvéolaires bénins à la plus forte concentration et des modifications non néoplasiques du nez et des poumons (inflammation, hyperplasie). Les études in vitro ont montré une métabolisation pulmonaire jusqu’à 100 fois plus rapide chez la souris que chez le rat, le hamster ou le singe, ce qui la rend beaucoup plus sensible aux effets pulmonaires du naphtalène.
Par voie orale, le rat (0 - 10 - 20 mg/kg/j, 6 j/sem. pendant 100 semaines) ne développe pas de tumeur.
Effets sur la reproduction [1, 10]
Le naphtalène ne provoque pas de modification dans les organes reproducteurs des rongeurs ; il est fœtotoxique à des doses fortement toxiques pour les mères.
Fertilité
Il n’y a pas d’étude propre aux effets du naphtalène sur la fertilité ; cependant, lors des études de cancérogenèse par inhalation, aucune modification histologique n’a été observée dans les organes reproducteurs de la souris (150 mg/m3) ou dans les testicules de rat (300 mg/m3, 90 jours).
Développement
La fœtotoxicité est observée à des doses provoquant une toxicité maternelle significative chez le rat (≥ 450 mg/kg/j, du 6e au 15e jour de gestation) et la souris (300 mg/kg/j, du 7e au 14e jour de gestation). La toxicité maternelle se manifeste également à des doses inférieures sans provoquer de fœtotoxicité. Il n’y a pas d’induction de malformation même aux fortes doses. Chez le lapin, au contraire, aucun effet fœtotoxique n’apparaît, même à des doses très toxiques pour les mères (≥ 200 mg/kg/j, du 6e au 18e jour de gestation).
-
Toxicité sur l’Homme [1, 2, 10, 11]
Chez l’homme, les effets constatés après exposition aiguë ou chronique sont essentiellement des symptômes digestifs, ainsi que ceux dus à une hémolyse. Ils sont particulièrement fréquents et sévères chez les personnes présentant un déficit en G6PD (glucose-6-phosphate déshydrogénase). Le produit est également susceptible d’entraîner des opacités du cristallin. Il est sans doute légèrement irritant pour la peau et l’œil.
Toxicité aiguë
L’ingestion est suivie de troubles digestifs (nausées, vomissements, douleurs abdominales et diarrhées). Pour des doses importantes sont susceptibles de survenir, en plus, des troubles de conscience pouvant conduire au coma convulsif.
Une hémolyse peut compliquer ce tableau chez les sujets ayant un déficit en glucose-6-phosphate déshydrogénase (G6PD) et se traduire par une insuffisance circulatoire aiguë et une néphropathie anurique. Une atteinte hépatique est exceptionnelle.
Un certain nombre d’articles signalent que le produit est irritant par voie cutanée chez l’homme. Les sources d’information ne sont cependant pas citées ou trouvables.
Il est aussi traditionnellement rapporté que le produit peut entraîner une irritation oculaire. L’étude des articles sources montre qu’il est plus signalé des opacités du cristallin.
Toxicité chronique
Quelques cas de malaises, de céphalées et de vomissements ont été rapportés après expositions répétées.
Plusieurs cas d’anémies hémolytiques ont été publiés suite à une exposition à des vapeurs de naphtalène, généralement chez des nouveau-nés. Certains présentaient un déficit en G6PD.
Une étude rapporte des effets oculaires parmi 21 ouvriers exposés par voie cutanée et atmosphérique durant une à cinq années. Des opacités du cristallin ont été observées chez huit d’entre eux. La plupart présentaient des opacités localisées périphériques, sans conséquence sur l’acuité visuelle. Deux étaient cependant porteurs d’une véritable cataracte. Il n’est pas précisé si la fréquence de ces effets était significativement différente de celle rencontrée dans la population générale. D’autres anomalies visuelles (diminution de l’acuité visuelle, choriorétinite...) ont été rapportées dans la littérature sans qu’il soit possible d’affirmer que ces effets sont dus au naphtalène.
Effets cancérogènes
Il n’existe pas d’étude épidémiologique publiée. Un article rapporte quatre cas de cancers du larynx chez des ouvriers travaillant dans la purification du naphtalène. Aucune conclusion ne peut en être tirée, ces personnes étant des fumeurs exposés à d’autres polluants.
Effets sur la reproduction
Deux cas de nouveau-nés présentant une anémie hémolytique ont été publiés. Leurs mères avaient été exposées par ingestion volontaire, à une dose probablement élevée, au naphtalène durant le 3e trimestre de la grossesse. Dans un cas, la mère présentait un déficit en G6PD, dans l’autre cette donnée n’était pas précisée mais elle présentait une anémie hémolytique.
-
Interférences métaboliques
-
Cohérence des réponses biologiques chez l'homme et l'animal
