Pathologie - Toxicologie
-
Toxicocinétique - Métabolisme [7, 8]
Après une absorption rapide, le styrène se distribue essentiellement dans les tissus adipeux; après métabolisation, il est éliminé surtout dans l’urine (sous forme d’acides mandélique et phénylglyoxylique) et, en faibles quantités, dans l’air expiré et les fèces.
Chez l'animal
Absorption
Le styrène est absorbé rapidement par toutes les voies et principalement par inhalation. Chez l’homme, l’absorption pulmonaire représente 60-70% de la concentration d’exposition; elle est proportionnelle à la concentration atmosphérique et à la durée d’exposition et augmente en cas d’exercice. L’absorption cutanée est faible (1 μg/cm2/ min). La pénétration par voie cutanée des vapeurs de styrène a été étudiée sur des volontaires humains. Elle s’avère négligeable par rapport à l’absorption par voie pulmonaire, représentant environ 5% de la dose totale absorbée.
Chez l’animal, l’absorption gastro-intestinale est identique à l’absorption pulmonaire, alors que la pénétration cutanée représente 9,4% de la concentration inhalée.
Distribution
Le pic sanguin est atteint en quelques minutes à 1 heure et le styrène ou ses métabolites sont distribués, chez le rat et la souris, essentiellement dans les tissus adipeux (demi-vie = 6,3 h), mais aussi dans les reins, le foie, le pancréas et le cerveau (demi-vie = 2 à 2,4 h). Chez l’homme, comme chez l’animal, il n’y a pas d’accumulation.
Métabolisme
Le styrène est complètement métabolisé (cf. schéma métabolique).
Schéma métabolique
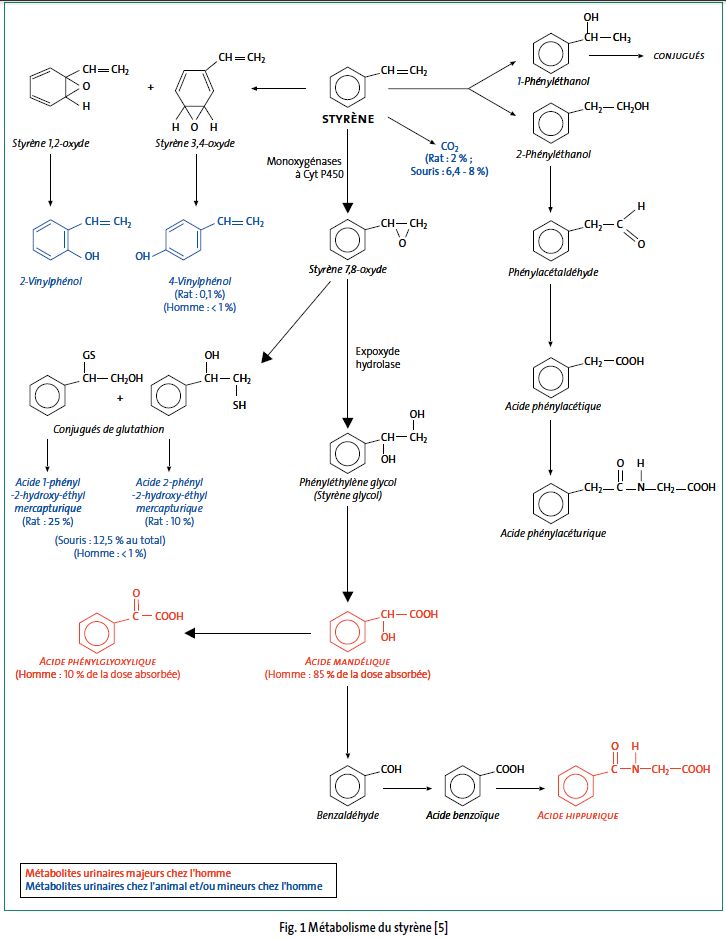
Excrétion
Chez l’animal, une dose orale est éliminée après 24 heures, essentiellement dans les urines (75% chez le rat, 63% chez la souris), dans l’air expiré sous forme inchangée (2-3%) et sous forme de CO2 (2% chez le rat et 6-8% chez la souris), ainsi que dans les fèces (4%).
Surveillance Biologique de l'exposition
Différents paramètres sont proposés pour évaluer l’exposition au styrène : styrène sanguin, urinaire et dans l’air expiré ; acides mandélique (AM) et phénylglyoxylique (PG) urinaires.
Le dosage du styrène urinaire en fin de poste de travail est le paramètre recommandé pour la SBEP Paramètre spécifique, sensible, le mieux corrélé aux concentrations atmosphériques, il reflète l’exposition au styrène du jour même.
Les taux d’acides mandélique (AM) et phénylglyoxylique (PG) urinaires, prélèvements réalisés en fin de poste de travail, reflètent l’exposition au styrène du jour même et des deux jours précédents. Ils ne sont pas spécifiques.
Le dosage du styrène sanguin immédiatement en fin de poste reflète l’exposition du jour même. Paramètre spécifique, il pose des difficultés d’ordre pré-analytique.
Le dosage du styrène dans l’air expiré immédiatement en fin de poste reflète l’exposition très récente mais ce prélèvement pose quelques difficultés.
Il existe des valeurs biologiques d’interprétation pour le styrène urinaire et les acides mandélique (AM) et phénylglyoxylique (PG) urinaires pour la population professionnellement exposée.
-
Mode d'actions
-
Toxicité expérimentale
Toxicité aiguë [7, 9]
Lors d’une exposition aiguë, le styrène est essentiellement un irritant du tractus exposé.
L’ingestion de styrène à forte dose provoque chez le rat une irritation sévère de l’œsophage et de l’estomac.
Par inhalation (rat, cobaye, 2500 ppm/10 h), le styrène agit sur le système nerveux central : faiblesse et torpeur, puis incoordination, tremblements et coma; la mort survient en 8 heures. Les effets sont sévères au niveau pulmonaire : irritation, congestion, œdème, hémorragie et infiltration leucocytaire.
Chez la souris, le styrène induit une irritation sensorielle avec une baisse de la fréquence respiratoire ; la RD50 est estimée entre 156 et 980 ppm selon la souche et la durée d’exposition. Il est également hépatotoxique, provoquant une augmentation de poids du foie (125 ppm, 6 h/j, 4 j) et une nécrose sévère des hépatocytes centrolobulaires (500 ppm/6 h).
L’application cutanée (500 ou 3000 mg/kg/j pendant 7 j) ne provoque aucun signe de toxicité locale ou systémique chez le rat.
Le styrène provoque, en application locale chez le lapin, une irritation cornéenne modérée avec des lésions réversibles et une légère irritation cutanée et, par inhalation, une irritation nasale.
Voie
Espèce
DL 50/CL 50
Orale
Rat
1 000 - 5 000 mg/kg
Souris
316 mg/kg
Inhalation
Rat
2 770 - 6 000 ppm/4 h
Souris
4 940 ppm/2 h
9 500 mg/m3/4 h (≈ 2 230 ppm/4 h)
Cobaye
5 200 ppm/4 h
Tableau I. DL 50/CL 50 du styrène.
Toxicité subchronique, chronique [7, 9]
En expositions répétées ou prolongées, le styrène est irritant et ototoxique.
Par voie orale chez le rat (1000 mg/kg/j, 5 j/sem., 28 j), le styrène est un irritant du tractus gastro-intestinal, provoquant la létalité ; à dose plus faible, il induit des modifications de poids des reins et du foie.
Par voie cutanée (pur, lapin, 20 applications, 4 sem.), c’est un irritant modéré avec légère nécrose.
Par inhalation, il provoque une irritation oculaire et nasale (rat, cobaye, ≥ 1300 ppm, 7 h/j, 7 mois), une augmentation de la susceptibilité à l’infection staphylococcique (rat, souris, 6,5 ppm, 4 h/j, 3 mois) ; le lapin et le singe ne présentent pas d’effet toxique à ces concentrations.
Le styrène est ototoxique chez le rat (300 ppm, 6 h/j, 5 j/sem., 4 sem.). Il provoque une perte auditive permanente essentiellement dans les fréquences moyennes (16 kHz) et moyennes-basses (3-4 kHz) ; les cellules ciliées externes de l’organe de Corti sont la cible principale. Cet effet ototoxique pourrait être potentialisé par l’éthanol qui altère le métabolisme du styrène. Lors d’expositions simultanées (rats, 6 h/j, 5 j/sem., 4 sem.) au styrène (750 ppm) et au bruit (97 dB), un effet synergique a été observé sur l’augmentation des seuils auditifs et des pertes cellulaires de la cochlée [10].
Effets génotoxiques [7, 11]
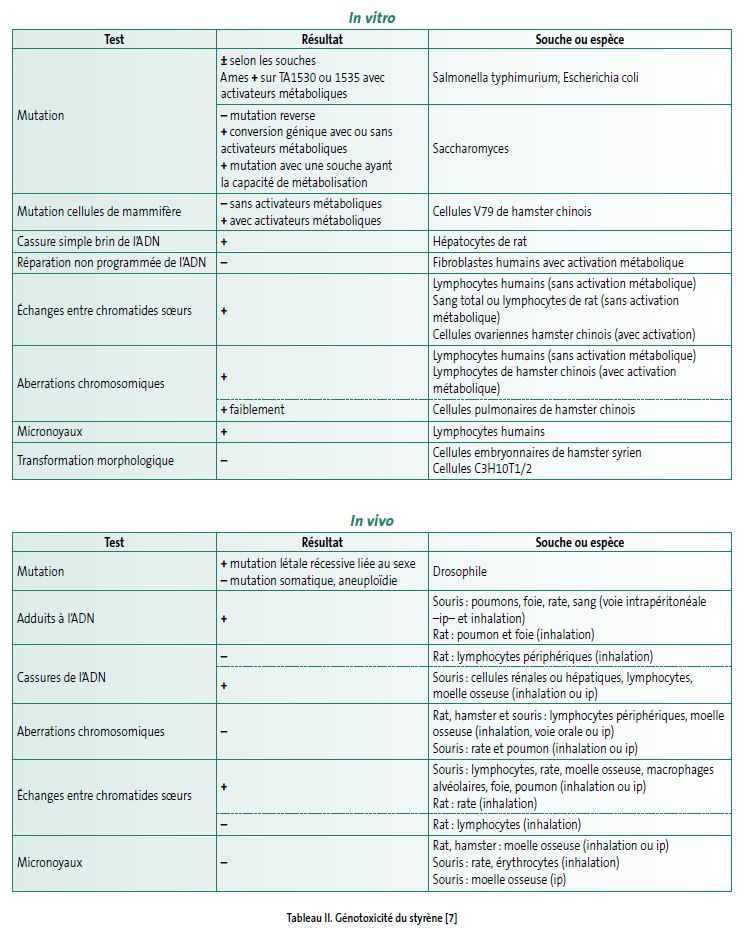
In vitro, le styrène est faiblement mutagène et clastogène après métabolisation; in vivo, il induit des adduits à l’ADN et des échanges entre chromatides sœurs, à forte concentration après plusieurs expositions. Son métabolite principal, le styrène-7,8-oxyde, se fixe à l’ADN, est mutagène et clastogène.
Le styrène possède un certain potentiel génotoxique in vitro et in vivo (voir tableau II) ; son métabolite principal, le styrène-7,8-oxyde, est considéré comme responsable de ces effets. Les lésions à l’ADN ainsi que la génotoxicité sont influencées par un polymorphisme génétique qui agit sur la quantité et l’activité des enzymes de détoxication de l’oxyde de styrène (époxyde hydrolase et glutathion S-transférase).
Effets cancérogènes [7, 12, 25]
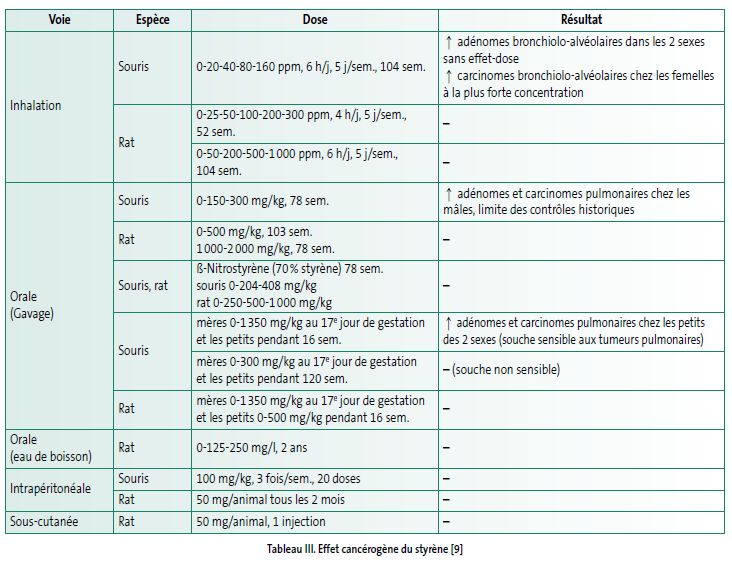
Le styrène est un cancérogène uniquement pour la souris (tumeurs pulmonaires) ; il n’y a donc qu’une évidence limitée d’un effet cancérogène du styrène chez l’animal bien que son métabolite principal (styrène-7,8-oxyde) soit considéré comme génotoxique et cancérogène pour l’animal. Depuis 2019, le CIRC (IARC) a classé le styrène dans le groupe 2A des agents porobablement cancérogènes pour l’homme.
L’effet cancérogène du styrène a été testé chez le rat et la souris, par voies orale, inhalatoire, intrapéritonéale et sous-cutanée (voir tableau III). Les lésions induites de l’ADN et la cytotoxicité pulmonaire sont les deux mécanismes possibles de l’effet cancérogène du styrène. Les différences de métabolisme entre espèces pourraient expliquer les différences de sensibilité. Les souris ont un taux de cytochrome P450 (2E1 et 2F2) plus important au niveau des cellules de Clara pulmonaires et synthétisent, localement, une quantité plus importante d’oxyde de styrène responsable de l’essor de la prolifération cellulaire.
Effets sur la reproduction [6, 7]
Des effets d'intensité variable sur le développement ont été mis en évidence selon les espèces animales. Par contre, aucun effet sur la fertilité chez le rat et n’est pas tératogène.
Fertilité [6]
Le styrène n’a montré aucune pathologie testiculaire par inhalation, jusqu’à 160 ppm chez la souris, 1000 ppm ou plus chez le rat, le lapin, le cobaye ou le singe. Par voie orale, il provoque, chez le rat (gavage, ≥ 400 mg/kg/j, 60 jours), une baisse du comptage spermatique et une modification des enzymes testiculaires et chez la souris (50mg/l dans l’eau de boisson, 4 sem.) une forte baisse du taux de testostérone plasmatique. Dans une expérience sur 3 générations (125-250 ppm dans l’eau de boisson), il n’a pas d’effet sur la capacité reproductrice du rat [13].
Développement [6]
Le styrène passe la barrière placentaire chez le rat et la souris ; chez le rat, la concentration sanguine fœtale atteint la moitié de celle du sang maternel. Chez le rat, les études par inhalation n’ont pas mis en évidence d’effets sur les paramètres de toxicité fœtale, classiquement examinés, en l’absence de toxicité maternelle et pour des doses pouvant atteindre 600 ppm. Toutefois, des retards neurologiques ou comportementaux ont été observés dans plusieurs études (non BPL et ne suivant pas les lignes directrices de l’OCDE), chez des animaux exposés à 300 ppm, sans toxicité maternelle concomitante. Une étude récente de reproduction sur 2 générations confirme ces résultats : les petits de la génération F2, exposés à la plus forte dose (500 ppm), présentent des signes de retard du développement postnatal avec une diminution du poids, un retard dans l’apparition des marqueurs de développement et de la séparation du prépuce et des atteintes du développement neuromoteur (baisse de l’aptitude à nager, léger retard dans l’activité motrice normale et diminution de la force d’agrippement des pattes antérieures). À cette dose, seule une légère toxicité maternelle est observée (légère diminution du poids et dégénérescence de l’épithélium nasal). Les nouveau-nés exposés à 150 ppm présentent seulement une diminution de leur poids pendant l’allaitement, sans aucune toxicité maternelle.
Par voie orale (≤ 300 mg/kg/j par gavage, du 6e au 15e jour de gestation), aucun effet sur le développement du rat n’est observé, même en présence de toxicité maternelle.
Des signes de toxicité pour le développement ayant été observés dans 3 études, le comité européen pour l'évaluation des risques (RAC) a conclu que le styrène devait être classé Repro 2, H361d.
-
Toxicité sur l’Homme [6, 7]
L'exposition à de fortes concentrations de styrène entraîne une irritation des muqueuses oculaire et respiratoire, les expositions chroniques irritent la peau et les muqueuses. Les effets aigus et chroniques portent principalement sur le système nerveux central : ébriété, troubles neurocomportementaux (dans certaines études), une altération de la vision de couleurs est signalée et dans une moindre mesure du nerf auditif. Des effets génotoxiques sont suspectés chez l'homme et les effets cancérogènes ne sont pas clairement établis (hémopathies) du fait de co-expositions. Il n'est pas possible de conclure quant à d'éventuels effets sur la reproduction.
Toxicité aiguë
Après inhalation, il est essentiellement constaté à partir d’expériences sur des volontaires :
- une atteinte du système nerveux central se traduisant par des céphalées, vertiges, somnolence, troubles de la coordination, asthénie lors d’exposition à 800 ppm environ (pour des concentrations plus fortes, un coma peut survenir). Des modifications aux tests psychomoteurs sont notées dès 200 ppm pour des périodes de 30 à 90 minutes d’exposition. Par contre, plusieurs études avec les mêmes tests montrent une absence d’effets pour des expositions de 20 à 150 ppm pendant 1 à 6 heures ;
- une irritation des muqueuses nasales est rapportée lors d’expositions de volontaires à 800 ppm pendant 3 heures. Aucun signe d’irritation n’est noté pour 100 ppm pendant 1 heure, les premiers symptômes apparaissant à 375 ppm.
Il y a peu de travaux de qualité sur l’homme concernant l’irritation cutanée. Il semble qu’une exposition unique n’entraîne pas de signe d’irritation cutanée.
L’exposition aux vapeurs de styrène engendre une sensation d’irritation oculaire dès 375 ppm pendant 1 heure d’exposition. En dessous de 200 ppm durant cette même période, il n’y a aucune sensation d’irritation. Une légère irritation survient au bout de 7 heures d’exposition à 100 ppm, ces effets sont qualifiés de forts à partir de 600 ppm. Dans tous les cas, il n’y a jamais eu d’examens ophtalmologiques objectivant ces effets.
Malgré une utilisation très large de ce produit, les cas rapportés de sensibilisation dans la littérature sont rarissimes. Un cas a été publié avec un patch test positif lors d’utilisation de plastiques.
Il en est de même pour la sensibilisation respiratoire. Deux cas d’asthme sont rapportés mais avec des incertitudes scientifiques.
Toxicité chronique
Toxicité sur le système nerveux
Par inhalation, l’exposition répétée engendre, sans que les niveaux d’exposition soient bien évalués, des symptômes d’atteinte du système nerveux central, tels que des céphalées, des nausées, des vertiges, des sensations ébrieuses, des pertes de l’équilibre ou des signes d’incoordination.
Un certain nombre d’examens complémentaires ont par ailleurs été effectués.
Les effets sur le système nerveux central ont été étudiés par la pratique d’EEG et de tests neurocomportementaux. Les études avec les EEG ne sont pas conclusives. Pour les tests neurocomportementaux, dans de très nombreuses études, des effets sont observés mais on ne peut discriminer s’ils sont dus à des expositions aiguës (notamment à une dépression du système nerveux central) ou à des expositions chroniques. Seules quatre études ont permis d’identifier des effets dus à la chronicité de l’exposition, mais leurs résultats sont ambigus : l’une montre une atteinte de la dextérité manuelle, l’autre une absence de déficit sur le temps de réaction, deux autres présentent des biais d’interprétation.
L’atteinte du système nerveux périphérique a été soupçonnée, bien que non démontrée cliniquement, et largement étudiée. Les résultats sont discordants montrant, pour certaines études, une diminution légère de la vitesse de conduction nerveuse et des résultats normaux pour d’autres.
Des effets sur l’audition ont été soupçonnés mais non démontrés par la pratique d’audiogrammes. Certaines études, bien que critiquées, semblent montrer un effet mineur sur les réflexes vestibulaires.
Une méta-analyse publiée en 2005 par Bénignus indique qu'il n'y a pas de relation entre les excrétions des métabolites urinaires du styrène et le temps de réaction simple des sujets. Il existe cependant une relation linéaire entre ces excrétions de métabolites et le temps de réaction avec choix ainsi que la discrimination des couleurs. Ces effets ne sont observés que pour des expositions supérieures à 20 ppm[14].
Des examens biologiques ont également été réalisés pour objectiver cette atteinte sur le système nerveux. Une diminution de l’activité de la dopamine ß–hydroxylase sérique et une augmentation de la prolactine sérique ont été retrouvées dans plusieurs études. Pour cette dernière, certains auteurs pensent qu’il s’agit plus d’une augmentation due à des expositions aiguës.
Autres effets
Par voie cutanée, des expositions répétées entraînent des irritations de la peau.
Par inhalation, une irritation oculaire, nasale et de la gorge est notée. Des signes d’irritation des voies aériennes inférieures sont également rapportés, sans anomalie des fonctions respiratoires aux épreuves fonctionnelles.
Des anomalies des constantes hématologiques, rénales et hormonales ont été rapportées dans certaines études. Elles sont cependant inconstantes, difficilement interprétables et ne sont pour l’instant pas retenues comme étant dues à une exposition au seul styrène. Certains auteurs rapportent une augmentation des gamma-glutamyl transférases sans autres signes d’anomalie hépatique.
Effets génotoxiques
De très nombreuses études ont été menées chez l’homme pour investiguer la survenue de mutation génique, notamment la recherche d’aberrations chromosomiques, de micronoyaux, d’échanges de chromatides sœurs, de cassures de brins d’ADN, d’adduits de l’ADN dans les lymphocytes périphériques dans l’industrie des plastiques renforcés aux fibres de verre.
Des niveaux très faibles d’adduits à l’ADN ont été retrouvés chez certains ouvriers, ainsi que des cassures d’ADN monobrin. Les études sur les échanges de chromatides sœurs se sont révélées négatives. Les études sur les mutations géniques, les aberrations chromosomiques, les micronoyaux donnent des résultats ambigus : 5 montrent que le styrène est faiblement clastogène, 11 sont clairement négatives. Aucune relation dose-réponse n’a été montrée.
Du fait des grandes variabilités retrouvées dans la population, ces résultats ne peuvent être analysés au niveau individuel.
Effets cancérogènes
Plusieurs études épidémiologiques, cas-témoins ou de cohortes, ont été effectuées dans les secteurs de la production de styrène monomère, dans la polymérisation du styrène, dans la production du SBR (caoutchouc styrènebutadiène) et dans la production de plastiques renforcés aux fibres de verre.
Dans cette dernière notamment, des études ont été bien menées avec des niveaux d’exposition au styrène assez importants et une absence d’exposition à d’autres produits chimiques. Ces études ne montrent pas de liens entre cancer et styrène.
On observe uniquement une augmentation des cancers des systèmes lymphatiques et hématologiques dans l’industrie de la production du caoutchouc styrène-butadiène. Une exposition au butadiène était généralement conjointe, cette augmentation a été mise sur le compte de ce dernier.
Effets sur la reproduction
Un certain nombre d’études épidémiologiques ont été publiées concernant la fertilité et le développement. Les résultats sont généralement négatifs et ne permettent pas d’établir de liens entre le styrène et des avortements spontanés, des malformations congénitales, des petits poids de naissance et des troubles des règles, de la fécondité, de la qualité du sperme.
Ces études concernent généralement des effectifs assez limités, avec des niveaux d’exposition industrielle relativement bas, ce qui ne permet pas de pouvoir conclure à une absence certaine d’effet.
-
Interférences métaboliques
-
Cohérence des réponses biologiques chez l'homme et l'animal
